En ce mois du cœur, le laboratoire du chercheur Rubén Marín Juez dévoile le premier atlas complet du développement des vaisseaux coronaires chez le poisson zèbre. Porté par l’étudiant Muhammad Abdul Rouf, ce travail d’envergure retrace, avec une résolution cellulaire inédite, la manière dont les vaisseaux se forment et interagissent avec le muscle cardiaque – couronnant plusieurs années d’analyses minutieuses.
Cartographier un cœur de poisson pour comprendre la malformation cardiaque d’un nouveau-né
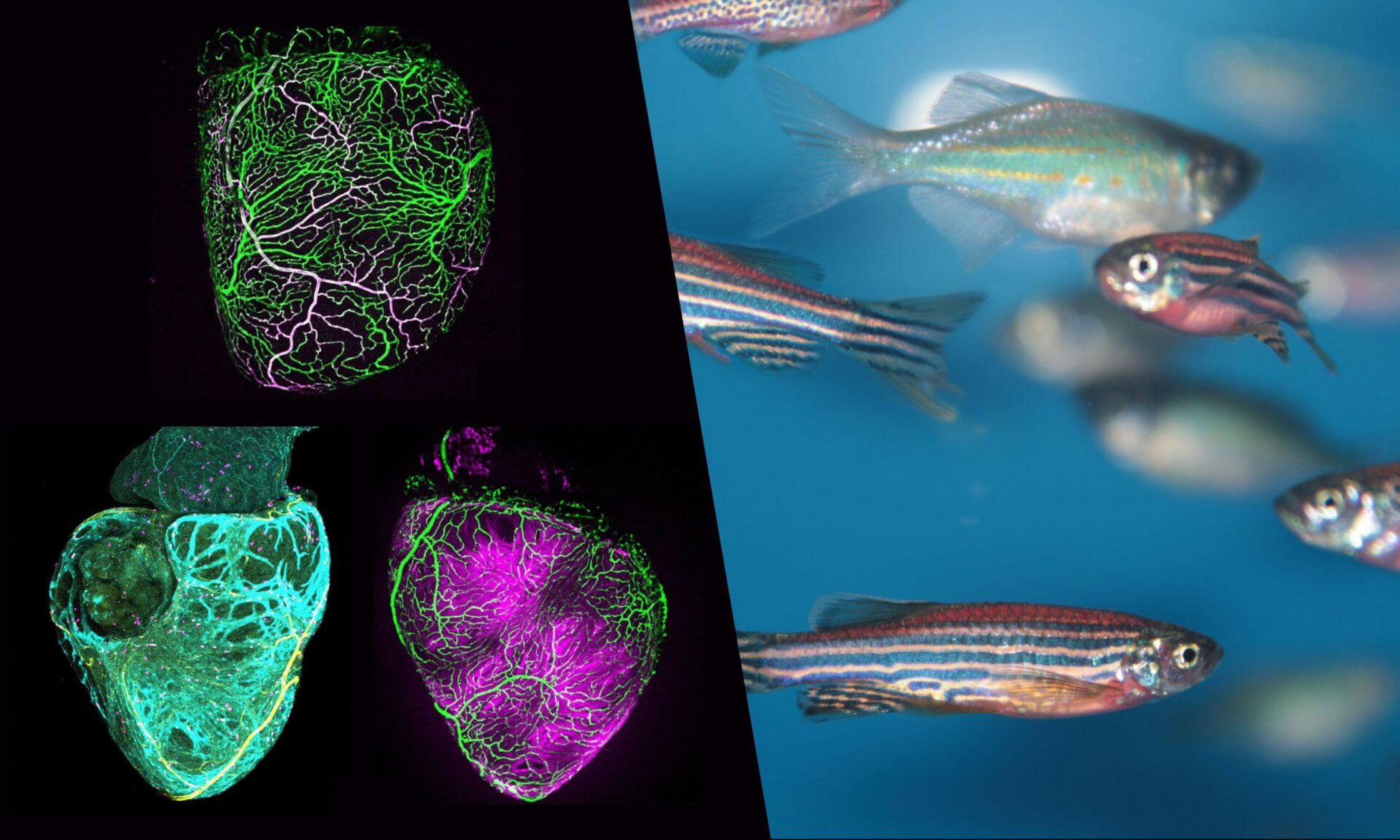
Une architecture révélée
L’étude, dont les résultats sont publiés dans la revue Development, combine l’imagerie 3D et des lignées génétiques de poissons zèbres afin de déterminer où, quand et comment les vaisseaux coronaires se forment et guident la maturation des cellules du muscle cardiaque.
«Pendant longtemps, les vaisseaux ont été vus comme de simples conduits qui transportent le sang. Aujourd’hui, nous démontrons qu’ils orchestrent la croissance du muscle cardiaque dès les premières étapes de la formation du cœur», souligne Rubén Marín Juez, chercheur au Centre de recherche Azrieli du CHU Sainte‑Justine et professeur à la Faculté de médecine de l’Université de Montréal.
Cette idée trouve son origine dans les travaux sur la régénération cardiaque menés par le laboratoire: chez le poisson zèbre adulte, les vaisseaux coronaires constituent un véritable échafaudage permettant la reconstruction du muscle après une lésion. Cette observation a amené l’équipe à remonter aux sources du développement embryonnaire pour comprendre comment ces interactions ont lieu dès le début de la vie.
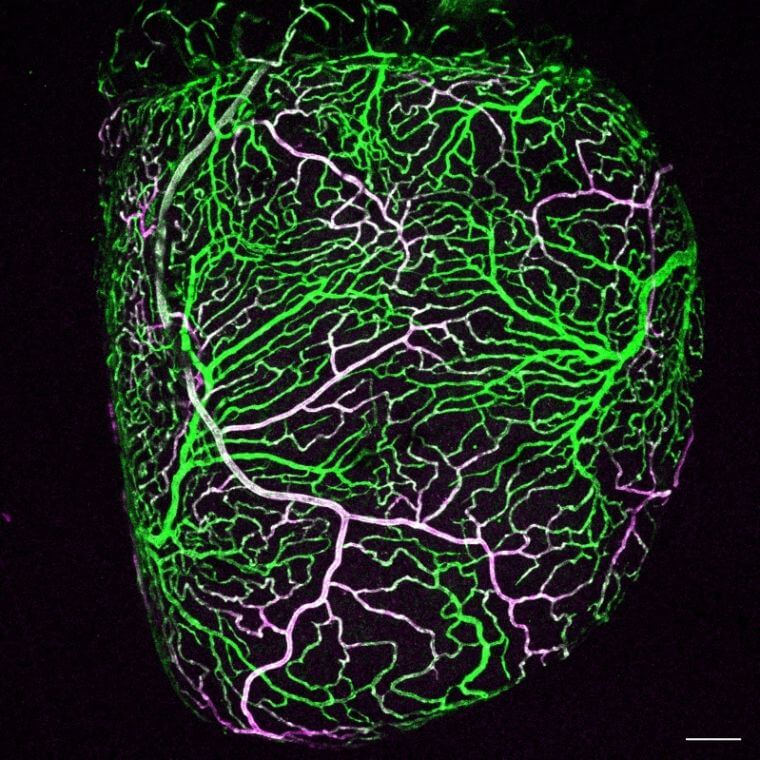
Une fenêtre unique sur le cœur en formation
Modèle de choix en biologie du développement, le poisson zèbre permet d’observer un cœur fonctionnel à peine 24 heures après la fécondation. Avec un accès direct aux embryons et larves de poisson, et un marquage des cellules facilité par leur transparence naturelle, l’équipe est en mesure d’examiner des structures qui sont invisibles chez le mammifère à ce stade de vie.
En analysant le développement vasculaire micromètre par micromètre, dès une taille corporelle de sept millimètres, l’équipe a produit des images 3D d’une précision remarquable. Grâce à cette approche, elle a pu suivre la formation du réseau coronaire: émergence des premières pousses vasculaires, ancrage, croissance, ramification et maturation en un réseau pleinement fonctionnel.
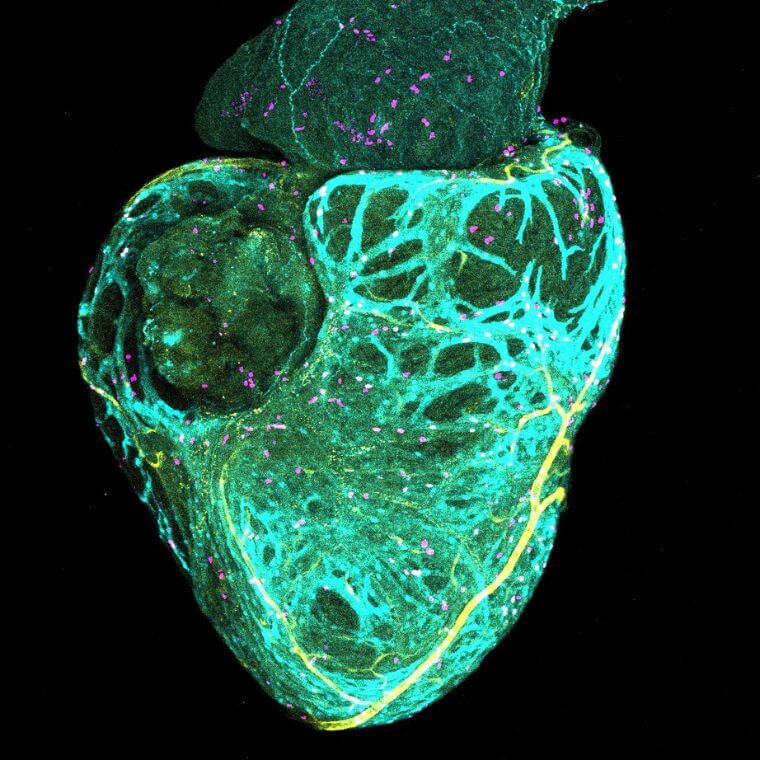
La comparaison entre les différents modèles de poisson zèbre a aussi révélé le moment exact où le développement se dérègle, mettant en évidence les défauts qui apparaissent lorsqu’un gène clé est altéré.
En parallèle, l’équipe a réalisé un séquençage de l’ARN sur plus de 37 000 cellules, ce qui a permis de mettre au jour divers types cellulaires associés ainsi que de nouveaux marqueurs et signatures moléculaires liés aux étapes clés du développement coronaire. Cet atlas offre ainsi un portrait complet, à la fois anatomique et génomique, de la mise en place du réseau coronaire.
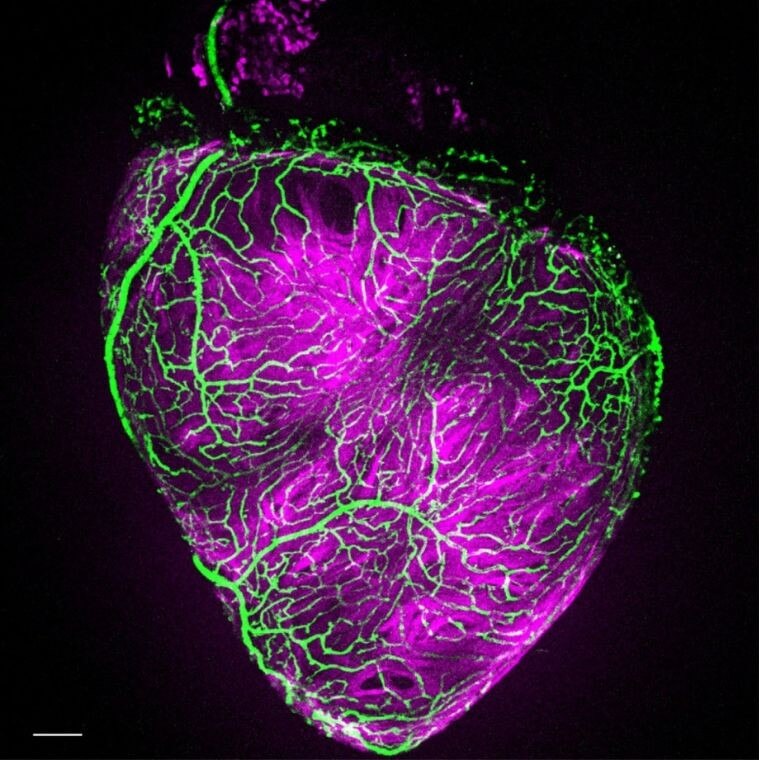
Une ressource pour comprendre les maladies cardiaques pédiatriques
Au-delà des avancées fondamentales, cet atlas ouvre la voie à une meilleure compréhension de plusieurs cardiopathies congénitales. De plus en plus d’indices donnent à penser qu’un réseau coronaire insuffisant ou désorganisé, très tôt dans le développement, peut compromettre la formation normale du cœur. Parce qu’elle est parvenue à cartographier ces étapes avec une grande finesse, l’équipe peut désormais explorer ces hypothèses avec une précision inégalée.
Chez des espèces capables de régénérer leur cœur, comme le poisson zèbre, plusieurs programmes du développement sont réactivés après une lésion. Comprendre ces mécanismes dès le stade embryonnaire pourrait donc inspirer de futures approches thérapeutiques, notamment en pédiatrie.
En combinant imagerie de pointe, génétique et analyses unicellulaires, cette étude illustre la force du partenariat entre équipes scientifiques et plateformes technologiques: une collaboration qui transforme notre compréhension du cœur dès ses premiers battements.